Opis
Badanie prekoncepcyjne CLARA — poznajcie swoje geny jeszcze przed ciążą
CLARA to nowoczesne, przesiewowe badanie genetyczne dla par, które starają się o dziecko lub dopiero planują ciążę. W prosty i bezpieczny sposób pozwala wykryć ryzyko poważnych chorób genetycznych, które, nawet zdrowi rodzice, mogą przekazać dziecku.
Dzięki łatwemu badaniu prekoncepcyjnemu zyskasz wiedzę, świadomie zaplanujesz ciążę, a w razie nieprawidłowych wyników – podejmiesz dalsze kroki ku szczęśliwemu i zdrowemu rodzicielstwu.
Zadbaj o przyszłość swojej rodziny – wyprzedź chorobę. Wybierz CLARA.
Czy badanie przesiewowe CLARA jest dla nas?
Badania przesiewowe (ang. carrier screening) to m.in. badania genetyczne dla par przed ciążą, które wykonuje się, aby ocenić ryzyko wystąpienia chorób genetycznych u dziecka.
Wasz pakiet badań przed ciążą nie powinien ich pomijać.
Wykonajcie badanie, jeśli….
- Planujecie zajść w ciążę teraz lub w przyszłości,
- Leczycie się z powodu niepłodności o niewyjaśnionej przyczynie,
- Jesteście objęci opieką i leczeniem w klinikach in-vitro – przygotowujecie się do zapłodnienia in vitro,
- Jesteś po licznych poronieniach samoistnych, które nie mają wyjaśnionego podłoża.
Co dają badania genetyczne dla par przed ciążą?
Wykonując badanie CLARA sprawdzicie, czy jesteście nosicielami najczęstszych chorób genetycznych występujących w populacji polskiej. Tym samym dowiecie się, czy istnieje ryzyko odziedziczenia konkretnej choroby przez Wasze dziecko.
Badanie możecie wykonać jeszcze przed podjęciem decyzji o założeniu lub powiększeniu rodziny.
Czy wiesz, że każdy z nas jest nosicielem co najmniej 5-6 mutacji?
Mutacje to zmiany w genach, które nie zawsze dają objawy chorobowe. Jeśli jesteśmy nosicielami mutacji, posiadamy tylko jedną kopię zmienionego genu. Nic nam nie dolega i nie mamy pojęcia o nosicielstwie.
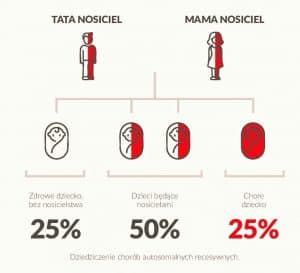
Jednak, jeśli Ty i Twój partner jesteście nosicielami tej samej mutacji w danym genie, to w przypadku części chorób genetycznych, pojawia się aż do 25% ryzyka, że Wasze dziecko będzie chore. Ten genetyczny bagaż przekazujemy dzieciom niezależnie od tego, ile mamy lat.
Dlatego badania przed zajściem w ciążę są tak ważne. Pozwalają poznać ryzyko i, jeśli trzeba, podjąć odpowiednie kroki, aby zwiększyć szansę na zdrowe i szczęśliwe rodzicielstwo.
Jakie są rozwiązania, jeśli Ty i Twój partner jesteście nosicielami?
- Jeśli wynik potwierdzi nosicielstwo, macie możliwość skorzystania z odpowiednich metod leczenia.
- Możecie świadomie wybrać inną formę zapłodnienia. Plan leczenia może obejmować – inseminację nasieniem dawcy, in vitro z dawstwem komórek jajowych lub przystąpienie do procedury in-vitro z dodatkową diagnostyką zarodka – (IVF + PGT-M – preimplantation genetic testing for monogenetic diseases)
- Dzięki tym rozwiązaniom, można zminimalizować ryzyko wystąpienia choroby u przyszłego dziecka, tej w kierunku której zostanie przeprowadzona diagnostyka zarodka – PGT-M.
Genetyczne badanie zarodka – PGT-M
- Świadomie przygotujecie się do odpowiedniego poprowadzenia ciąży (badania prenatalne potwierdzające lub wykluczające ryzyko wystąpienia choroby); zaplanujecie właściwe leczenie chorego dziecka.
Co badamy w panelu?
Panel CLARA optima został stworzony z przede wszystkim z myślą o parach pochodzenia polskiego.
Obejmuje on wykrycie nosicielstwa najczęstszych chorób genetycznych, z uwzględnieniem najczęstszych mutacji w populacji słowiańskiej.
Istotne jest, aby panele nosicielstwa wykonała para, ponieważ ryzyko wystąpienia danej choroby u dziecka jest szacowane dla pracy planującej potomstwo.
CLARA to również przykład badania dla mężczyzn przed ciążą. Przyszły tata też ma duży wpływ na zdrowie swojego dziecka.
| NOSICIELSTWO JEDNOSTKI CHOROBOWEJ |
GEN |
BADANE MUTACJE |
|---|---|---|
| Mukowiscydoza |
CFTR |
delF508, del2,3 |
| Rdzeniowy zanik mięśni (SMA) |
SMN1 |
delecja eksonu 7 |
| Zespół łamliwego chromosomu X |
FMR1 |
mutacja dynamiczna (CGG)n (badanie przesiewowe) |
| Niedosłuch wrodzony |
GJB2 |
c.35delG, c.35G>T, c.35G>A |
| Fenyloketonuria |
PAH |
c.1222C>t |
| Niedobór dehydrogenazy długołańcuchowych kwasów tłuszczowych (LCHADD) |
HADHA |
c.1528G>C |
| Niedobór dehydrogenazy acylo-CoA średniołańcuchowych kwasów tłuszczowych (MCADD) |
ACADM |
c.985A>G |
| Zespół Smitha-Lemliego-Opitza (SLOS) |
DHCR7 |
c.976G>T, c.452G>A, c.452G>C |
| Zespół Nijmegen |
NBN |
c.657_661del5 |
| Deficyt białka SCO2 (choroba mitochondrialna) |
SCO2 |
c.418G>A |
| Zespół Leigha (choroba mitochondrialna) |
SURF1 |
c.312_321del10insAT, c.845_846delCT |
Panele CLARA zostały stworzone na podstawie wiedzy klinicznej i laboratoryjnej z wykorzystaniem doświadczeń różnych ośrodków genetyki medycznej w Polsce. Są zgodne z rekomendacjami niżej wymienionych stowarzyszeń.
- Amerykańskie Towarzystwo Ginekologów i Położników zaleca, aby informować o możliwości wykonania badania prekoncepcyjnego (carrier screening) każdą kobietę planującą ciążę lub będącą w ciąży.
- Zgodnie z rekomendacjami ESHG (Europejskiego Towarzystwa Genetyki Człowieka) oraz ACMG (Amerykańskiego Kolegium Genetyki Medycznej i Genomiki) w skład panelu powinny wchodzić choroby o znanym obrazie klinicznym, a więc takie których znane są objawy chrakteryzujące samą chorobę oraz stopień jej zaawansowania. Wartość kliniczna paneli nosicielstwa jest istotniejsza niż liczba przebadanych genów.
| JEDNOSTKA CHOROBOWA |
CHARAKTERYSTYKA |
|---|---|
| Mukowiscydoza |
Najczęściej występująca na świecie choroba genetyczna skutkująca skróceniem życia. W przebiegu tej choroby dochodzi do zaburzenia funkcji gruczołów zewnątrz wydzielniczych, co prowadzi do niewydolności związanych z nimi narządów, przede wszystkim układów oddechowego oraz pokarmowego. |
| Rdzeniowy zanik mięśni (SMA) |
Druga najczęściej występująca choroba genetyczna skutkująca skróceniem życia. Polega na postępującym obumieraniu neuronów w rdzeniu kręgowym co prowadzi do osłabienia siły mięśni. Choroba może objawiać się w różnym wieku, jednak w około 70% przypadków pierwsze symptomy pojawiają się w okresie niemowlęcym lub wczesnym dzieciństwie. Obecnie SMA jest możliwe do wyleczenia dzięki zastosowaniu terapii genowej określanej mianem najdroższego leku świata. Jej koszt wynosi miliony złotych i nie jest objęta refundacją NFZ. |
| Zespół łamliwego chromosomu X |
Tzw. pełna mutacja (od 200 powtórzeń CGG) to jedna z najczęstszych przyczyn niepełnosprawności intelektualnej oraz objawów spektrum autyzmu uwarunkowanych genetycznie. Premutacja (zakres powtórzeń 55 – 199) wiąże się z ryzykiem przedwczesnego wygasania czynności jajników u kobiet (POI – ang. premature ovarian insufficiency). Ze względu na dynamiczny charakter mutacji nosicielstwo zwiększonej liczby powtórzeń trójnukleotydowych wiąże się z ryzykiem zwielokrotnienia do zakresu pełnej mutacji w kolejnym pokoleniu, co skutkuje wystąpieniem u dziecka zespołu łamliwego chromosomu X (FXS). |
| Niedosłuch wrodzony |
Niedosłuch jest jedną z najczęstszych chorób narządów zmysłów, natomiast gen GJB2 jest najważniejszym z dotychczas poznanych genów odpowiedzialnych za powstawanie niedosłuchu izolowanego. Mutacja c.35delG odpowiada za ok. 80% przypadków wrodzonego niedosłuchu spowodowanego mutacjami w genie GJB2. |
| Fenyloketonuria |
Chorobą metaboliczna prowadząca do gromadzenia się w organizmie fenyloalaniny. Z uwagi na defekt metabolizmu fenyloalaniny konieczne jest stosowanie diety eliminacyjnej niskofenyloalaninowej. W przypadku nieprzestrzegania diety bądź jej zbyt późnego wprowadzenia dochodzi do nieodwracalnych zmian neurorozwojowych takich min. upośledzenie rozwoju umysłowego oraz motorycznego. |
| Niedobór dehydrogenazy długołańcuchowych kwasów tłuszczowych (LCHADD) |
Wada genetyczna często określana jako „gen kaszubski” ze względu na częste występowanie mutacji w tej populacji. W przebiegu choroby dochodzi do nagłych spadków glukozy we krwi (np. po intensywnym wysiłku fizycznym, infekcji, której towarzyszą wymioty i biegunka lub podczas dłuższych przerw w jedzeniu). Gdy organizm nie może czerpać energii z posiłków zaczyna wykorzystywać własne kwasy tłuszczowe. Mutacja genu HADHA, odpowiedzialna za ich deficyt mu to jednak uniemożliwia. Niedobór LCHAD jest chorobą potencjalnie śmiertelną, jednak zdiagnozowany można leczyć za pomocą diety oraz unikania głodzenia. |
| Niedobór dehydrogenazy acylo-CoA średniołańcuchowych kwasów tłuszczowych (MCADD) |
Jest wrodzonym defektem mitochondrialnego utleniania kwasów tłuszczowych. Choroba ta charakteryzuje się szybko postępującym załamaniem metabolicznym, które często objawia się hipoglikemią hipoketotyczną, letargiem, wymiotami, drgawkami i śpiączką. Charakteryzuje się 25% ryzykiem zgonu przy pierwszym epizodzie. Podobnie jak w przypadku LCHAD należy unikać głodzenia. |
| Zespół Smitha-Lemliego-Opitza (SLOS) |
Mutacje w genie DHCR7 powodują brak lub zmniejszenie aktywności enzymu reduktazy 7-dehydrocholesterolu, co prowadzi do zahamowania szlaku endogennej syntezy cholesterolu w organizmie lub do zmniejszenia powstawania cholesterolu. Zespół ten charakteryzuje duża zmienność obrazu klinicznego, od postaci letalnych po łagodne. Objawem dominującym jest niepełnosprawność intelektualna, często w stopniu głębokim oraz zespół wad wrodzonych m.in. mózgu, serca, przewodu pokarmowego, nadnerczy, narządów płciowych zewnętrznych, a także cechy dysmorfii, m.in. małogłowie (mikrocefalia) i zrośnięcie palców (syndaktylia). Obecnie w Polsce, w stosunku do częstości nosicielstwa odnotowuje się zbyt małą liczbę rozpoznań choroby, co wiązane jest z niezdiagnozowaniem postaci łagodnych i atypowych, ale także prawdopodobnie wysoką letalnością w okresie płodowym oraz śmiertelnością w noworodkowym. Przypuszcza się, że SLOS jest jedną z najczęstszych chorób metabolicznych w populacji polskiej. |
| Zespół Nijmegen |
Choroba wywołana mutacjami w genie NBN kodującym nibrynę, białko biorące udział w mechanizmie naprawie pęknięć w dwuniciowym DNA zapewniając tym samym utrzymanie stabilności chromosomowej i integralności genomu. Na skutek mutacji w genie NBN dochodzi do zaburzeń naprawy DNA predysponujących do spontanicznych pęknięć chromosomów i ich rearanżacji. W konsekwencji choroba ta charakteryzuje się znaczną skłonnością do występowania nowotworów złośliwych, zwłaszcza glejaków i chłoniaków. Ponadto, choroba objawia się wewnątrzmacicznym opóźnieniem wzrastania płodu, a następnie zaburzeniem wzrastania, a także niedoborem odporności i cechami dysmorfii jak małogłowie czy mikrognacja. Większość dzieci umiera w pierwszej dekadzie życia z powodu nowotworów. Zespół ten występuje najczęściej w populacjach słowiańskich, co w 90% przypadków uwarunkowane jest założycielską mutacją c.657_661del5, określaną jako “mutacja słowiańska”, zwiększoną predyspozycję do powstawania nowotworów obserwuje się także u heterozygotycznych nosicieli mutacji. |
| Deficyt białka SCO2 (choroba mitochondrialna) |
Choroby mitochondrialne to schorzenia wynikające z zaburzeń w funkcjonowaniu i strukturze mitochondriów spowodowanych mutacjami w genomie mitochondrialnym lub jądrowym DNA kodującym białka specyficzne dla mitochondriów i regulujące ich działanie. Jednymi z częściej występujących defektów genetycznych są mutacje w genach SURF1 (zespół Leigha) i SCO2 (deficyt białka SCO2). Objawy chorób mitochondrialnych u dzieci są niespecyficzne i obejmują zestaw postępujących zmian w mózgu, mięśniach, gruczołach wydzielania wewnętrznego, narządach zmysłów (głuchota, oftalmoplegia) i innych tkankach i narządach. Co związane jest z faktem, iż mitochondria są organellami dostarczającymi komórkom energię niezbędną do ich prawidłowego funkcjonowania. |
| Zespół Leigha (choroba mitochondrialna) |
Bezboleśnie
Szybko i łatwo
Bez wychodzenia z domu
Badanie dostarczone do Ciebie w ciągu 24h.
Wynik badania w ciągu 14 dni.
Wynik możesz skonsultować z genetykiem w INVICTA
Badania wykonywane jest z DNA pochodzącego ze śliny.
Jak to działa?

CZY ŚLINA JEST DOBRYM MATERIAŁEM?
Dowiedz się, dlaczego badanie genetyczne ze śliny jest tak samo wiarygodne jak badanie z krwi – BADANIE ZE ŚLINY – WSZYSTKO CO POWINIENEŚ WIEDZIEĆ.



Opinie
Na razie nie ma opinii o produkcie.